فروش هیپوکلریت کلسیم
برای استعلام قیمت، خرید مواد شیمیایی و تهیه پودر هیپوکلریت کلسیم از راههای ارتباطی زیر اقدام کنید و از بهترین کیفیت مواد شیمیایی دکتر کمیکال برخوردار شوید.
تلفن ثابت: 02166568403
واتساپ: 09124666706
هیپوکلریت کلسیم چیست؟
هیپوکلریت کلسیم یک ترکیب شیمیایی با فرمول Ca(ClO)2 است. معمولاً به آن پودر سفید کننده یا اکسی کلرید کلسیم هم میگویند. این ترکیب معمولاً به عنوان پودر سفید کننده شناخته میشود. همچنین به عنوان اکسی کلرید کلسیم، کلرید آهک یا نمک کلسیم هیپوکلرو اسید نیز شناخته می شود.

کلسیم هیپوکلریت یک ترکیب یونی است که از یک کاتیون کلسیم (Ca2+) و دو آنیون هیپوکلریت (ClO–) ساخته شده است. با وجود اینکه اکسی کلرید کلسیم در دمای اتاق کاملاً پایدار است، به آرامی در محیطهای مرطوب تجزیه میشود و بوی مشخصی دارد که آن را به اسم بوی «کلر» میشناسیم.
اکسی کلرید کلسیم به شکلهای بی آب و هیدراته به صورت تجاری در دسترس است و یکی از مواد اصلی پودر کلر و پودر سفید کننده است. Ca(ClO)2 در مقیاس صنعتی از طریق واکنش گاز کلر با این ترکیب تولید میشود. معادله شیمیایی این واکنش در زیر ارائه شده است:
2Ca(OH)2 + 2Cl2 → Ca(ClO)2 + H2O + CaCl2
به طور کلی، پودر سفید کننده مخلوطی از هیپوکلریت کلسیم، به صورت (Ca(ClO2).2Ca(OH)2) و کلرید کلسیم (CaCl2.2Ca(OH)2) است. از آنجایی که Calcium Hypochlorite حاوی دو یون ClO– است، این ترکیب در مقایسه با اکسی کلرید کلسیم (NaOCl) کلر بیشتری ارائه میدهد.
ساختار کلسیم هیپوکلریت
ساختار مولکول Ca(ClO)2 در زیر نشان داده شده است که از یک یون Ca+ و دو یون ClO- تشکیل شده است که از یک یون Ca+ و دو یون ClO- تشکیل شده است:
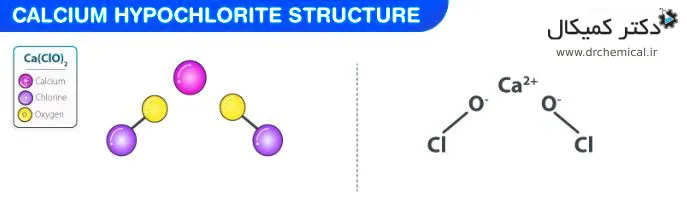
هر یون کلریت دارای بار 1- است در حالی که یون کلسیم دارای بار 2+ است. بنابراین یک کاتیون کلسیم می تواند با دو یون هیپوکلریت پیوند یونی ایجاد کند.
ویژگی های فیزیکی هیپوکلریت کلسیم
- هیپوکلریت کلسیم یک جامد سفید/خاکستری در دمای اتاق است
- حلالیت آن در آب 21 گرم در 100 میلیلیتر است و پس از حل شدن با آب واکنش نشان میدهد
- حلالیت آن در آب سخت در مقایسه با حلالیت آن در آب نرم نسبتاً کم است
- Ca(ClO)2 بوی قوی کلر دارد (زیرا با مولکولهای آب موجود در هوا واکنش میدهد)
ویژگی های شیمیایی کلسیم هیپوکلریت
| Calcium Hypochlorite
|
Ca(ClO)2 |
| جرم مولکولی | 142.98 گرم بر مول |
| چگالی | 2.35 گرم بر سانتی متر مکعب |
| نقطه ذوب | 100 درجه سانتی گراد |
| نقطه جوش | در 175 درجه سانتی گراد تجزیه می شود |
واکنش های اکسی کلرید کلسیم
- کلسیم هیپوکلریت به عنوان یک باز قوی عمل میکند؛ زیرا وقتی در آب حل شود به راحتی H+ را میپذیرد، آنیون هیپوکلریت یک پروتون از H2O میپذیرد و یک یون OH- آزاد میکند. واکنش شیمیایی به صورت زیر خواهد بود:
ClO– + H2O → HClO + OH–
- این ترکیب همچنین یک عامل اکسید کننده قوی است زیرا میتواند به راحتی یک الکترون را بپذیرد.
- کلسیم هیپوکلریت با اسید هیدروکلریک واکنش داده و کلرید کلسیم (CaCl2)، آب و گاز کلر (Cl2) تولید میکند. معادله شیمیایی این واکنش به صورت زیر است:
4HCl + Ca(ClO)2 → CaCl2 + Cl2 + H2O
کاربرد اکسی کلرید کلسیم یا سفید کننده
ترکیب Ca(ClO)2 اغلب برای ضد عفونی کردن حجم زیادی از آب استفاده میشود. همچنین به طور گسترده از اکسی کلرید کلسیم در استخرها برای ضدعفونی کردن آب و از بین بردن میکروبهای موجود در آن استفاده میکنند. برخی از کاربردهای دیگر Calcium Hypochlorite در زیر ذکر شده است:
- از آنجایی که این ترکیب یک عامل اکسید کننده خوب است، این ترکیب در زمینه شیمی آلی بسیار مفید است.
- برای بدست آوردن آلدئیدها/اسیدهای کربوکسیلیک با شکستن پیوندهای موجود در گلیکولها و اسیدهای کتو استفاده میشود.
- Ca(ClO)2 همچنین میتواند در واکنش تولید کلروفرم استفاده شود.
- از این نوع ترکیب میتوان برای ضد عفونی کردن فاضلاب و آب آشامیدنی استفاده کرد زیرا در آب کلر زیادی آزاد می کند.
(فروش مواد شیمیایی تصفیه آب و فاضلاب)
خطرات کلرید کلسیم
ماهیت خورنده هیپوکلریت را به یک ماده خطرناک تبدیل میکند که باید با دقت نگهداری شود. باید در محیط سرد و خشک نگهداری شود و نباید در معرض هیچ فلز یا اسیدی قرار گیرد. اگر هر اسیدی با اکسی کلرید کلسیم تماس پیدا کند، بخارهای بسیار سمی گاز کلر تولید میشود.











میلاد عظیمی –
سلام خسته نباشید، تفاوت هیپوکلریت کلسیم با سدیم چیه؟
عظیم زاده –
سلام خسته نباشید
ما میخواستیم نسبت به خرید هیپوکلریت کلسیم برای ضدعفونی اب استخر اقدام کنیم اما دوتا سوال داشتیم از خدمتتون
کلسیم هیپوکلریت کلر پارس بهتره یا برند خارجی؟
قرص کلر بهتره یا پودر کلر؟