بررسی مکانیسم خوردگی فلزات
خوردگی فلزات یعنی چه؟
فرایند خوردگی فلزات واکنشی تدریجی، خود به خودی و پیوسته است و اغلب از سطح فلز آغاز میشود و تا درون آن نفوذ میکند. کنترل آن از سه جنبه ایمنی، اقتصادی و کاهش مصرف منابع طبیعی حائز اهمیت است. از آنجا که فرایند خوردگی با سرعت کم رخ میدهد، میتوان با آن مقابله کرد. با این وجود هر سال خوردگی خسارات جبرانناپذیری را به سامانههای مختلف به ویژه سامانههای فلزی وارد میکند.
خوردگی، از بین رفتن یک جسم بر اثر عوامل فیزیکی و شیمیایی محیط اطراف خود تعریف میشود. تمام اجسام، چه فلزی و چه غیرفلزی، در طبیعت دچار تخریب میشوند. ولی خوردگی اصطلاحی است که بیشتر در مورد فلزات به کار برده میشود. سرعت خوردگی اجسام فلزی بسیار بیشتر از غیرفلزاتی نظیر پلاستیک، سنگ، چوب و غیره است.
یکی از مثالهای ساده برای این واکنش، زنگ زدن آهن است که لایهای به رنگ زرد مایل به قهوهای روی سطح آهن ایجاد میشود. یک قطعه در حضور عوامل خورنده موجود در محیط رطوبت و اکسیژن خورده میشود، ولی اگر پوشش محافظ در برابر خوردگی روی این قطعه قرار گیرد، فرایند خوردگی، به راحتی اتفاق نمیافتد.
این واکنش شیمیایی فرایندی خود به خودی است که منجر به تولید گونههای پایدارتر از نظر سطح انرژی میشود. برای مثال، فلز آهن در محیط حاوی اکسیژن و رطوبت، آهن اکسید تولید میکند که در حالت طبیعی پایدارتر از فلز آهن است. همانند آهن، اغلب فلزات تمایل دارند تا به ترکیبات پایدارتر خود تبدیل شوند.
فلزات در اثر خوردگی با محیط اطراف خود واکنش میدهند و به ترکیبات پایدار مانند اکسید، سولفید یا کربنات تبدیل میشوند. این فرایند تدریجی اما پیوسته است و اغلب از سطح فلز آغاز میشود و تا درون آن نفوذ میکند و از آنجا که با سرعت کم رخ میدهد، لذا میتوان با آن مقابله کرد. اغلب این فرایندها در محیط های مایع یا گاز صورت میگیرند و تنها در برخی شرایط خاص، واکنش خوردگی جامد/جامد اتفاق میافتد. خوردگی جامد/جامد بین دو فلز در حال لغزش و ارتعاش اتفاق میافتد و در اثر سایش حفره و شیار ظاهر میشود.
این نوع واکنش در اجزای موتورها، قطعات خودرو و جزایی که به هم متصل شدهاند، و یا در تماس هستند، مشاهده میشود. خوردگی در هر نوع و در هر شرایط، در مقیاس اتمی و مولکولی رخ می دهد که با چشم غیرمسلح (بدون میکروسکوپ) قابل مشاهده نیست. بنابراین بررسی عملی خوردگی در این مقیاس امکانپذیر نیست.

دلایل ایجاد خوردگی فلزات
عوامل ایجاد خوردگی فلزات
- خوردگی فلزات با اسید
- خوردگی فلزات با حرارت
- خوردگی فلزات با نمک
- خوردگی فلز به علت ماهیت مواد
اصول خوردگی
از جمله اصول خوردگی عبارتند از:
- اصول ترمودینامیکی
- اصول الکتروشیمیایی
اصول ترمودینامیکی خوردگی
اصول ترمودینامیکی و الکتروشیمیایی نقش مهمی در تعیین رفتار خوردگی مواد ایفا میکنند. ترمودینامیک جهت خود به خودی یک واکنش شیمیایی را نشان میدهد. این برای تعیین اینکه آیا خوردگی به لحاظ نظری امکانپذیر است یا نه، استفاده میشود.
اصول الکتروشیمیایی خوردگی
اصول الکتروشیمیایی برای تعیین رفتار خوردگی مواد استفاده میشود. واکنش خوردگی را میتوان با واکنشهای جزئی مانند اکسیداسیون فلز و کاهش برخی از گونههای قابل احتراق محیط نشان داد، که هر دو به طور همزمان با سرعت برابر در پتانسیل مخلوط واکنش رخ میدهد. واکنش خوردگی به طور عمده در حد واسط بین فلز و محیط پیرامونش اتفاق می افتد.
طبیعت الکتروشیمیایی خوردگی را میتوان با حمله آهن در اسید هیدروکلریک نشان داد. وقتی آهن در اسید غوطهور میشود، فعالیت شدیدی انجام میشود؛ که در نتیجه این فعالیت گاز هیدروژن تکامل یافته و آهن حل میشود. واکنش زیر نشاندهنده این فعالیت است:

واکنش آند کاتد
واکنش بالا به دو واکنش اکسایش و کاهش تقسیم میشود:
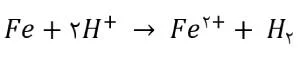
واکنش خوردگی
نظریه های خوردگی فلزات
نظریههای خوردگی ممکن است به نظریههای (۱) همگن و (۲) ناهمگن طبقهبندی شوند.

نظریه های خوردگی فلزات
نظریه همگن خوردگی
سطح ناهمگونی فلز باعث ایجاد روند خوردگی میشود. واگنر و تراود (۱۹۳۸) تاکید کردند که شرط لازم برای خوردگی، انحلال فلز و واکنش الکترونی است که در حد واسط فلز-محیط رخ میدهد. فلزات به علت واکنش انتقال باری که در حد واسط بین فلز و محیط پیرامونی رخ میدهد، ناپایدار میشوند.
بنابراین لازم است که اختلاف پتانسیل در سطح حد واسط منفی تر از پتانسیل تعادلی برای واکنش انحلال فلز (آنودیک) باشد یا مثبتتر از پتانسیل تعادل برای واکنش الکترون (کاتدی) باشد. این نظریه در توضیح خوردگی فلزات خالص و خوردگی یکنواخت مفید است، زیرا مکانهای کاتدی و آنودیک اغلب ویژگی خود را تغییر میدهند.
نظریه ناهمگن خوردگی
با توجه به این نظریه، حضور ناخالصیها در سطح فلز ضروری است و بنابراین یک سل نوعی بین مناطق کاتدی و آنودی تنظیم میشود. به دلیل واکنشهای الکتروشیمیایی که در میان فلزات فلزی و یونهای رسانا یا الکترولیت انجام میشود، فلز بیثبات میشود و از این رو خوردگی رخ میدهد.
بنابراین یک فلز خورده شده شامل:
- یک ناحیه اشباع از الکترون که در آن واکنش رها شدن الکترون اتفاق می افتد
- منبع الکترون که در آن یک واکنش الکترونی رخ می دهد
- یک هادی یونی برای نگه داشتن جریان جاری یونی
این مدل پایهای برای نظریه سل نوعی در مورد خوردگی و خوردگی ناهمگن است.

انواع خوردگی فلزات
انواع خوردگی در فلزات
اهميت روزافزون نقش دانش خوردگي در بهبود حفظ تاسيسات صنعتي و كاهش خطرات ناشي از آن، ضرورت آشنايي با مسايل پايهاي خوردگي را براي طيف هاي گوناگون دست اندركاران صنعتي دو چندان ميسازد. مرسوم ترین طبقه بندی انواع خوردگی بر اساس شكل ظاهري فلز خورده شده است. در اين تقسيم بندي هشت نوع خوردگي به شرح زير به عنوان مهمترين انواع خوردگي برشمرده شدهاند.
خوردگی یکنواخت چیست؟
اين نوع خوردگي به عنوان نوعي از خوردگي كه به صورت يكنواخت از ضخامت ماده كم ميكند تعريف شده است.
خوردگی دو فلزی
زماني كه دو فلز غير همجنس كه در تماس الكتريكي با يكديگر هستند، در معرض يك محلول هادي قرار ميگيرند، فلز مقاومتر خورده نميشود، اما آهنگ خوردگي فلز فعالتر كه مقاومت خوردگي كمتري دارد، افزايش مييابد. به علت وجود جريانهاي الكتريكي بين فلزات غيرهمجنس، اين نوع خوردگي، گالوانيك يا دو فلزي ناميده ميشود.
خوردگی بین دو دانه ای
در اين نوع خوردگي مرزدانه نسبت به خود دانه از سطح انرژي بالاتري برخوردار بوده و در نتيجه از نظر شيميايي فعالتر و نسبت به خوردگي حساستر است. خوردگي موضعي و متمركز در مرز دانهها يا نواحي نزديك به آنها در حاليكه خود دانهها خورده نشدهاند يا اينكه به مقدار اندکی خورده شدهاند، را خوردگي بين دانهاي مينامند.
جدایش انتخابی
جدايش انتخابي نوعي خوردگي است كه در آن عناصر خاصي از آلياژ، حل شده و از آن جدا ميشوند. روي، آلومينيوم، كبالت، نيكل و كروم از معمولترين عناصري هستند كه به اين طريق از آلياژ جدا مي شوند.

خوردگی سایشی چیست
خوردگی سایشی
خوردگي سايشي عبارتست از افزايش سرعت خوردگي يا از بين رفتن يک فلز در اثر حركت نسبي بين يک مايع خورنده و سطح فلز. در اين فرايند يونهاي فلزي حل شده روي سطح فلز، در اثر حركت سيال روي سطح باقي نمانده و يا محصولات جامد حاصل از خوردگي از سطح فلز به طريق مكانيكي جدا ميشوند.
خوردگی توأم با تنش
اين پديده عبارت است از ترک خوردن در اثر خوردگي توأم با تنش كه نتيجه اعمال همزمان تنشهاي كششي و محيط خورنده روي فلز است. در اين شرايط ترکهاي ريزي كه ناشي از فرايندهاي خوردگي موضعي هستند، به داخل فلز يا آلياژ پيشرفت ميكنند.
خوردگی شیاری
اين نوع خوردگي در بيشتر مواقع در شيارهايي كه در معرض محيط خورنده قرار دارند منجر به خوردگي موضعي شديدي ميشود.
خسارت هیدروژنی
خسارت هيدروژني يک اصطلاح كلي است كه دلالت بر خسارت مكانيكي وارد شده به فلز در اثر وجود يا واكنش با هيدروژن دارد كه خود به سه گروه تاول زدن هيدروژني، تردي هيدروژني و خوردگي هيدروژني تقسيمبندي ميشود. ترک خوردگي ناشي از هيدروژن نوعي از ترک است كه توسط اتمهاي هيدروژن كه به داخل فولاد نفوذ كرده و در داخل ساختار فلز تركيب شده و مولكولهاي هيدروژن تشكيل دادهاند، ايجاد ميشود.

محیط های خورنده
محیط های خوردگی فلزات
نوع خوردگی، واکنشهای خوردگی و سرعت خوردگی مواد به شددت تحت تاثیر محیط اطراف آنها قرار دارد. آب، خاک، جو و گازهای خشک جزء محیطهایی هستند که در مطالعات خوردگی بسیار حائز اهمیت هستند که به هر یک از آنها اشاره خواهد شد.
آب
بسیاری از سازههای مهم نظیر مخازن آب گرم و سرد، لولهها، اتصالات، شیرها، پمپها، مبدلهای گرمایی، دیگهای بخار، توربینها، کشتیها، ساختمانها و سازههای ساحلی و… در معرض خوردگی ناشی از آب قرار دارند.
عاملهایی که روی خوردگی فلزات در محیط های آبی موثر هستند عبارتاند از:
- غلظت اکسیژن حل شده
- دما
- مقدار PH
- نمکهای معدنی حل شده در آب
- مواد آلی
- جلبکها و باکتریها
- شدت جریان آب (و بی آب)
آب دریا الکترولیتی است که به صورت طبیعی حاوی غلظت بالایی از نمکهای مختلف به ویژه سدیم کلرید است به همین دلیل یکی از خورندهترین محیطهای طبیعی برای فلزات به حساب میآید.
جو
خوردگی جوی عبارت از خوردگی مواد در تماس با هوا و آلودگیهای خودروها و کارخانجات صنعتی است. آلودگیهای گازهای خروجی خودروها، پالایشگاهها و نیروگاه ها عمدتاً از گازهای گوگردیوکسید یا گوگرد تریوکسید و انواع اکسیدهای نیتروژن و کربن مونوکسید هستند که در اثر تماس با رطوبت هوا سبب ایجاد بارانهای اسیدی میشوند. بارانهای اسیدی سبب از بین رفتن بسیاری از ساختارهای فلزی موجود در فضای آزاد مثل قطعات فلزی مورد استفاده در ساختمانها مانند نمای ساختمان، درها، چارچوبها، پنجرهها، ناودانها و شیروانیها و همچنین قطعات فلزی پلها، دکلهای برق و بدنة خودروها میشوند.
گازهای خشک
واکنش بین فلز و هوا یا اکسیژن در غیاب فاز آبی، سبب اکسایش سطح فلز میشود. افزایش دما نقش مهمی در فرایند اکسایش ایفا میکند. اغلب خوردگیهای این دسته در دماهای بالا چشمگیر و محسوس می شود: بنابراین به خوردگی دمای بالا نیز معروف است. آلیاژهای مورد استفاده در توربینهای گازی، موتورهای جت، کورههای صنایع پالایش و پتروشیمی مواردی هستند که نیاز به انتخاب آلیاژ مناسب و طراحی دقیق در دماهای بالا دارند. اکسیژن، بخار گوگرد، کلر و آمونیاک گونههایی هستند که حتی در شرایط خشک سبب خوردگی فلزات میشوند.
خاک
بسیاری از تاسیسات فلزی در زیر زمین مدفون هستند و در معرض تاثیر خورنده خاک قرار دارند. برای مثال، در اثر خوردگی لولههای اصلی آبرسانی و فاضلاب ساخته شده از فولاد و چدن، مقدار زیادی از محتویات آنها در اثر نشت هدر میرود. سوراخ شدن لولههای فولادی انتقال گاز طبیعی دفن شده در زیر زمین در اثر فرایند خوردگی میتواند باعث آتشسوزی شده و منفجر شوند.
برخی دیگر از خسارات خوردگی در خاک عبارتاند از:
الف) مخازن فولادی نفت و بنزین که در زیر زمین نگهداری میشوند باید از خوردگی محافظت شوند تا نشت آنها به محیط زیست آسیب نزند.
ب) خوردگی در پایه دکلهای انتقال نیرو، علاوه بر هزینههای مستقیم تعمیر خسارات خوردگی و نیز احتمال فرو افتادن دکلهای فشار قوی به سبب خوردگی، میتواند منجر به آشفتگی جدی در توزیع برق یک منطقه شود.
ج) تیرهای فولادی تاسیسات، مثل پلها و سازههایی که درون خاک قرار دارند، مستعد خوردگی و فرو ریختن میباشند. عوامل موثر بر خوردگی خاک عبارتاند از: رطوبت، مقدار PH خاک، پتانسیل اکسایش کاهش، حضور نمکها، فعالیت میکروبی و غیره.
پیشنهاد دکتر کمیکال برای مطالعه بیشتر: خوردگی در صنایع نفت و گاز
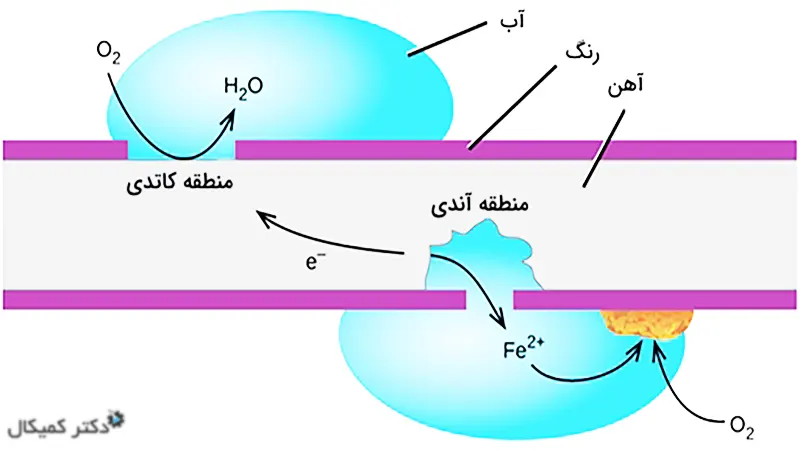
خوردگی فلز
فروشگاه مواد شیمیایی دکتر کمیکال تامین کننده مواد شیمیایی ضدخوردگی مورد نیاز صنعت میباشد. برای کسب اطلاعات بیشتر در مورد نحوه خرید مواد شیمیایی و قیمت با کارشناسان بخش فروش در تماس باشید.
محصولات ویژه:



